El protón es una de las partículas subatómicas llamadas nucleones. Con el neutrón, constituye el núcleo de los átomos. No es una partícula elemental porque consiste en tres partículas más pequeñas llamadas quarks. Estos están unidos entre sí por la fuerza nuclear fuerte descrita por ecuaciones similares a las del electromagnetismo.
Indice De Contenidos
¿Qué es el Protón?
El protón es una partícula cargada positivamente. Esta carga es en valor absoluto idéntica a la del electrón y la de su antipartícula cargada negativamente, el antiprotón . Los quarks que forman el protón, dos quarks arriba y un quark down llevan cargas eléctricas cuyos valores son fracciones de la carga eléctrica elemental del protón y el electrón
El protón es una partícula subatómica que lleva una carga elemental positiva
Los protones están presentes en los núcleos , generalmente relacionados con neutrones por la interacción fuerte (la única excepción, sino la de la isótopo más común, es el núcleo de hidrógeno ( protium 1 H), un solo protón). El número de protones de un núcleo está representado por su número atómico Z
El protón no es una partícula elemental: está compuesto de tres partículas unidas, dos quarks up y una quark down, lo que lo convierte en un barión
En el marco del modelo estándar de la física de partículas , y también experimentalmente en el estado actual de nuestro conocimiento, el protón también es estable en el estado libre, fuera de cualquier núcleo atómico. Algunas extensiones del modelo estándar predicen una inestabilidad (extremadamente débil) del protón libre
Las Propiedades del Protón
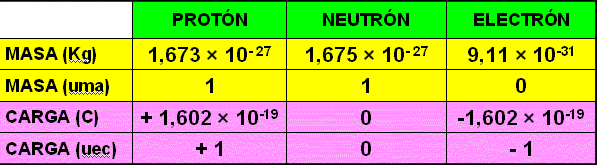
La masa del protón es de aproximadamente 938.2721 MeV / c 2 en unidad de energía adecuada para la física de partículas que equivale a 1.672 649 × 10 -27 kg . Esta masa se debe en gran medida a la energía intercambiada en forma de gluones entre los quarks y no se debe casi a sus masas ni a la existencia del bosón de Higgs. Esta masa se puede calcular con las ecuaciones de QCD, pero esto requiere supercomputadoras.
Al igual que el neutrón, el electrón y los quarks, el protón es un fermión que lleva un momento cinético intrínseco, un giro , que vale la mitad de la unidad dada por la constante de Planck. Es parte del grupo de los hadrones , las partículas sensibles a las interacciones fuertes. Estas fuerzas confinan a los quarks en los protones para que no puedan observarse como partículas libres, lo que ha llevado a pensar por un momento que los protones eran partículas elementales.
Por lo que sabemos, un protón aislado es estable, aunque algunas de las llamadas teorías de la Gran Unificación, GUT , predicen lo contrario, pero solo después de un tiempo extremadamente largo. Por otro lado, ciertos núcleos pueden desintegrarse al dar un neutrón, un positrón y un neutrino debido a la existencia de la fuerza nuclear débil. (Ver Articulo: Neutrón)
Descubrimiento del Protón
El término “protón” comenzó a usarse ampliamente en la literatura científica a partir de 1920 debido al trabajo y las propuestas de Rutherford, quien había descubierto la existencia del núcleo de los átomos y luego demostró que contenían núcleos de hidrógeno.
Ahora, ya en 1815, el químico y médico británico William Prout acababa de proponer la hipótesis de que todos los átomos se formaban a partir del átomo de hidrógeno, que había bautizado con el nombre de la antigua prosa griega que significa “primero”, basado en el hecho de que sus masas parecían ser múltiplos enteros de la masa del átomo de hidrógeno. Recordando la hipótesis de Prut, Rutherford acuñó los nombres “protón” y “proutón”.
Carga y Masa
La relación masa-carga es una cantidad física ampliamente utilizada en la electrodinámica de partículas cargadas, es decir, en óptica electrónica y óptica de iones. Se utiliza en campos científicos de la litografía, el microscopio electrónico, los tubos de rayos catódicos, los física de acelerador de la física nuclear de la espectroscopía de Auger de la cosmología y espectrometría de masas.
La importancia de esta noción radica en el hecho de que, según la electrodinámica clásica, dos partículas de la misma relación masa-carga siguen en el vacío una trayectoria idéntica cuando están sujetas a los mismos campos eléctricos y magnéticos.
Cuando las partículas cargadas se mueven en campos magnéticos y eléctricos, se aplican las siguientes dos leyes:
- F = Q (E+v x B) (ley de las fuerzas de lorentz)
- F = ma (Segunda ley del movimiento de Newton)
donde: - F representa la fuerza aplicada al ion,
- m , la masa de la partícula,
- una aceleración
- Q , la carga,
- E , el campo eléctrico,
- y v x B , el producto vectorial de la velocidad del ion y el campo magnético.
Usando la Tercera Ley del Movimiento de Newton , estas ecuaciones se convierten en:
- (m/Q)a = E + v x B
Esta ecuación diferencial es la ecuación clásica de movimiento de una partícula cargada en un vacío. Si uno también conoce las condiciones iniciales de la partícula, esta ecuación determina su movimiento en el espacio y en el tiempo. Por lo tanto, inmediatamente parece que dos partículas que tienen la misma relación m / Q se comportan de la misma manera en condiciones iniciales idénticas. Por esta razón, esta relación es una cantidad física significativa en campos científicos donde las partículas cargadas interactúan con campos magnéticos ( B ) o eléctricos ( E ). (Ver Articulo: Iones)
Historia
En el xix XX siglo, la relación masa a carga de ciertos iones se midieron por métodos electroquímicos. En 1897, la relación de carga a carga, [ m / e ] , del electrón se midió primero por JJ Thomson. Al hacerlo, mostró que el electrón, cuya existencia se había postulado anteriormente para explicar la electricidad, era en realidad una partícula con una masa y una carga; también demostró que su relación masa-carga era mucho menor que la del ión hidrógeno H +
En 1898, Wilhelm Wien.separados los iones en función de su masa a carga ración de un aparato óptico con iones sobre la que aplicar campos magnéticos y eléctricos. En 1901, Walter Kaufmann midió el aumento de masa relativa de electrones rápidos. En 1913, Thomson midió la relación de masa de carga iónica con un instrumento que denominó un espectrógrafo parabólico 5 . Hoy en día, el instrumento para medir la relación masa-carga se llama espectrómetro de masas. (Ver Articulo: Isotopos)
Relación de masa de carga
La relación masa-carga (m / q) de un objeto es, como su nombre lo indica, su masa dividida por su carga eléctrica . Esta cantidad generalmente solo es útil para objetos que pueden tratarse como partículas. Para objetos más grandes, la carga total, la densidad de carga, la masa total y la densidad de masa son frecuentemente más útiles.
Significado
En algunos experimentos, la relación masa-carga es la única cantidad que se puede medir directamente. A menudo sucede que la carga se puede inferir de consideraciones teóricas, por lo que este informe proporciona un medio para deducir la masa.
La relación de masa a carga a menudo se puede determinar a partir de la observación de las deflexiones de una partícula cargada en un campo magnético externo. La ecuación del ciclotrón , en combinación con otra información como la energía cinética de la partícula, proporciona la relación masa a carga. El espectrómetro de masas es una aplicación de este principio. El mismo principio se puede utilizar para extraer información de experimentos que utilizan cámaras de niebla .
La relación de fuerzas electrostáticas y gravitacionales entre dos partículas es proporcional al producto de su relación masa-carga. Se deduce que a nivel subatómico, las fuerzas gravitacionales son insignificantes.
El Electrón
El cociente de la carga del electrón por su masa, es una cantidad en física experimental. Tiene cierta importancia porque es difícil medir directamente la masa del electrón, en cambio, se deriva de mediciones de la carga fundamental. También tiene un significado histórico: la medida de Thomson lo convenció de que los rayos catódicos eran partículas que hoy reconocemos para los electrones.
El valor recomendado por el Comité de Datos de Ciencia y Tecnología (CODATA) de 2006 es CODATA se conoce como el cociente de carga de masa del electrón , pero el término relación se usa comúnmente.
En 1897, JJ Thomson logró calcular el “q / m” de un electrón, e incluso más exitosamente, utilizó el método de Dunnington, que combina el momento angular y la desviación generada por un campo magnético perpendicular.
Aparte de los métodos de JJ Thomson y Dunnington, existen otros dos métodos comunes para medir la relación masa-carga de un electrón:
1. Un método de magnetrón: el uso de una válvula de GRD7 ( válvula de Ferranti (en) ), el electrón de un filamento de tungsteno incandescente es expulsado a un ánodo. Luego se desvía por medio de un solenoide . Los valores de la corriente en el solenoide y en la válvula Ferranti permiten el cálculo de e / m.
2. El método del tubo de rayos finos: el electrón se acelera de un cátodo a un ánodo en forma de sombrero. El electrón es expulsado hacia un tubo de rayos lleno de helio, produciendo un círculo luminoso. El radio de este círculo permite el cálculo de e / m.
El efecto Zeeman
También se puede medir la relación de masa de carga de un electrón con el efecto Zeeman, que produce saltos de energía en presencia de un campo magnético B.